OAK BROOK, Ill. — Un modelo de IA entrenado para detectar anormalidades en imágenes de resonancia magnética de mama representó con precisión las ubicaciones de los tumores y superó a los modelos de referencia cuando se probó en tres grupos diferentes, según un estudio publicado en Radiology.

“La resonancia magnética asistida por IA podría potencialmente detectar cánceres que los humanos no detectarían de otro modo”, dijo el investigador principal del estudio, Felipe Oviedo, Ph.D., analista de investigación sénior en AI for Good Lab de Microsoft.
La mamografía de detección se considera el estándar de atención para la detección del cáncer de mama. Sin embargo, es menos efectiva en pacientes con mamas densas. La densidad mamaria es un factor de riesgo independiente para el cáncer de mama y puede enmascarar un tumor. Los médicos pueden solicitar una resonancia magnética mamaria como complemento a la mamografía de detección en mujeres con mamas densas y en aquellas con alto riesgo de cáncer.
![Figura 1. Resumen del método. (A) El diagrama muestra la detección profunda de anomalías explicables en la resonancia magnética de mama. Se pasa una proyección de intensidad máxima (MIP) de una mama a un modelo de red neuronal completamente convolucional entrenado mediante una función de pérdida de detección de anomalías explicable (descripción de datos completamente convolucional [FCDD]). (B) El diagrama muestra una comparación conceptual entre la clasificación binaria y la detección de anomalías: el sombreado representa los espacios de características normales (azul) y anormales (rojo) aprendidos, y los puntos representan casos individuales normales (azul) y anormales (rojo).](https://diagnosticojournal.com/wp-content/uploads/2025/07/390-RSNA-PR-MR-Figura-01-800.jpg)
“La resonancia magnética es más sensible que la mamografía”, dijo el Dr. Oviedo. “Pero también es más cara y tiene una mayor tasa de falsos positivos”.
Para mejorar la precisión y la eficiencia de la resonancia magnética mamaria de cribado, el equipo de investigación del Dr. Oviedo colaboró estrechamente con investigadores clínicos del Departamento de Radiología de la Universidad de Washington para desarrollar un modelo explicable de IA para la detección de anomalías. Los modelos de detección de anomalías distinguen entre datos normales y anormales, señalando las anomalías o anormalidades para su posterior investigación.
“Los modelos desarrollados previamente se entrenaron con datos de los cuales el 50% correspondía a casos de cáncer y el 50% a casos normales, lo cual representa una distribución muy poco realista”, afirmó el Dr. Oviedo. “Estos modelos no se han evaluado rigurosamente en poblaciones de baja prevalencia de cáncer o de cribado (donde el 2% de todos los casos son cáncer o menos), y además carecen de interpretabilidad, dos aspectos esenciales para su adopción clínica”.
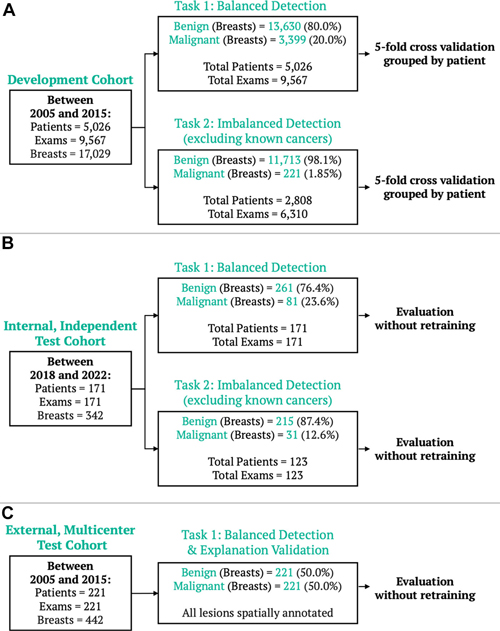
Para abordar estas limitaciones, los investigadores entrenaron su modelo utilizando datos de casi 10 000 exámenes consecutivos de resonancia magnética de mama con contraste realizados en la Universidad de Washington entre 2005 y 2022. Las pacientes eran predominantemente blancas (más del 80 %) y el 42,9 % tenía mamas heterogéneamente densas, mientras que el 11,6 % tenía mamas extremadamente densas.
“A diferencia de los modelos tradicionales de clasificación binaria, nuestro modelo de detección de anomalías aprendió una representación robusta de casos benignos para identificar mejor las neoplasias malignas anormales, incluso si están subrepresentadas en los datos de entrenamiento”, afirmó el Dr. Oviedo. “Dado que las neoplasias malignas pueden presentarse de múltiples maneras y son escasas en conjuntos de datos similares, el tipo de modelo de detección de anomalías propuesto en el estudio es una solución prometedora”.
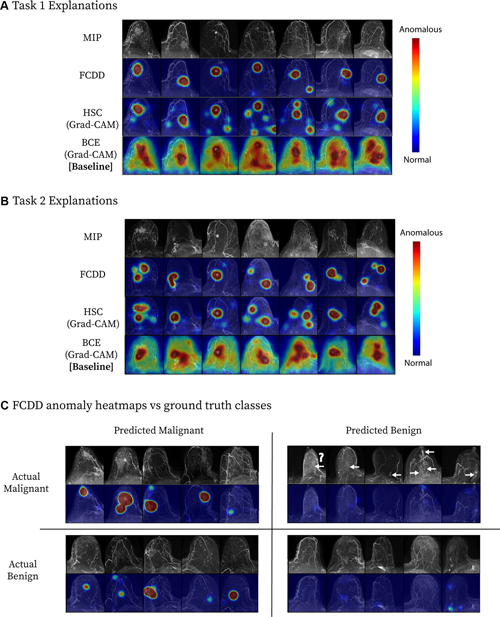
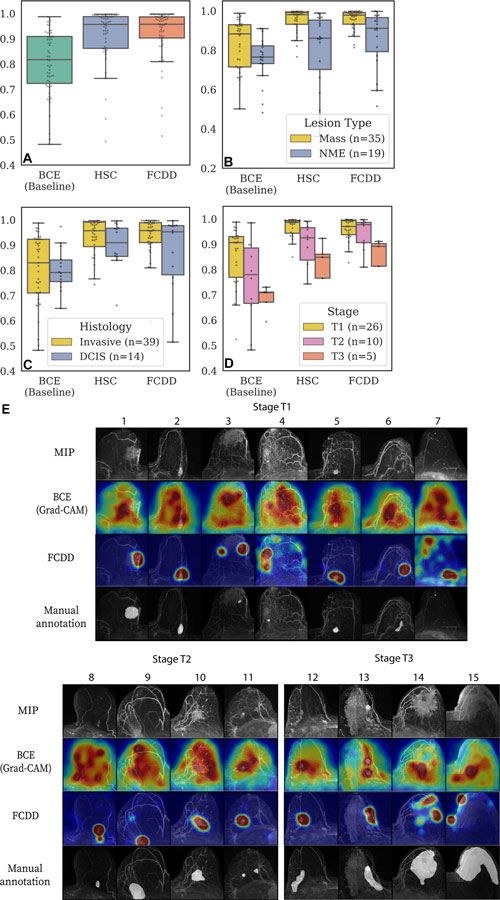
Además de proporcionar una puntuación de anomalía estimada, el modelo de detección genera un mapa de calor con resolución espacial para una imagen de RM. Este mapa de calor resalta en color las regiones de la imagen que el modelo considera anormales. Las regiones anormales identificadas por el modelo coincidieron con las áreas de malignidad comprobada por biopsia, anotadas por un radiólogo, superando ampliamente el rendimiento de los modelos de referencia.
El modelo se probó con conjuntos de datos internos y externos. El conjunto de datos interno consistió en resonancias magnéticas realizadas a 171 mujeres (edad media de 48,8 años) para cribado (71,9 %; 31 cánceres confirmados mediante biopsia posterior) o evaluación preoperatoria de un cáncer conocido (28,1 %; 50 cánceres confirmados mediante biopsia). El conjunto de datos externo, multicéntrico y de acceso público, incluyó resonancias magnéticas de mama previas al tratamiento de 221 mujeres con cáncer de mama invasivo.
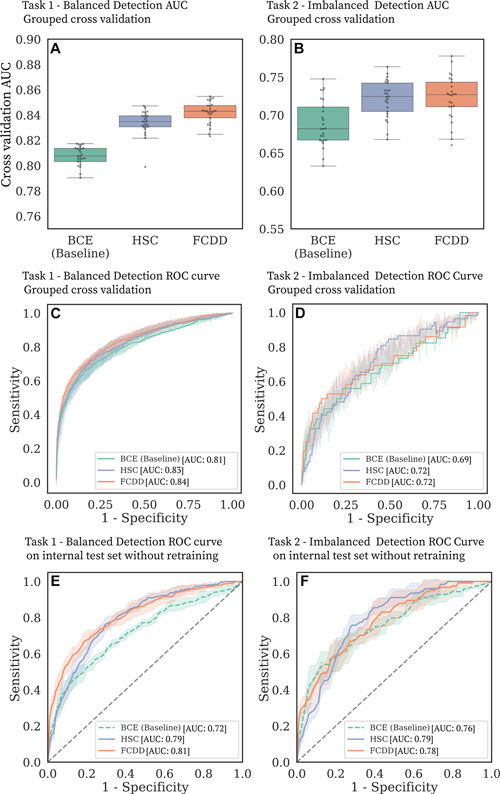
El modelo de detección de anomalías representó con precisión la ubicación del tumor y superó a los modelos de referencia en la validación cruzada agrupada, en conjuntos de datos de prueba internos y externos, y en tareas de detección equilibradas (alta prevalencia de cáncer) y desequilibradas (baja prevalencia de cáncer).
El Dr. Oviedo afirmó que, si se integra en los flujos de trabajo de radiología, el modelo de detección de anomalías podría potencialmente excluir exploraciones normales para fines de triaje y mejorar la eficiencia de la lectura.
“Nuestro modelo proporciona una explicación comprensible, a nivel de píxel, de las anomalías en una mama”, afirmó. “Estos mapas de calor de anomalías podrían identificar áreas potencialmente preocupantes, lo que permitiría a los radiólogos centrarse en los exámenes con mayor probabilidad de ser cancerosos”.
Antes de su aplicación clínica, dijo que el modelo necesita ser evaluado en conjuntos de datos más grandes y estudios prospectivos para evaluar su potencial para mejorar el flujo de trabajo de los radiólogos.

