La biopsia quirúrgica luego de la marcación radiológica con guías metálicas y/o colorantes, fue la forma habitual de investigar las lesiones sospechosas de malignidad, no palpables, detectadas mediante mamografía durante muchos años1.
En 1990 el Dr. Steve Parker publicó su experiencia inicial con biopsias histológicas con guía estereotáxica2. Fueron 103 biopsias, las primeras 30 se realizaron con un equipo que se agregaba al mamógrafo (add-on), en la era de la mamografía analógica.
La paciente estaba sentada, veía el procedimiento, el espacio para que operara el radiólogo entre la cabeza de la paciente y la mama era escaso y luego de cada exposición mamográfica había que revelar las placas (al menos 3 minutos), por lo que las posibilidades que la paciente se moviera (atentando contra la precisión y certeza de la obtención del material) o de reacción vagal no eran despreciables.
Esto motivó que las siguientes 73 biopsias se realizaran en un equipo dedicado solamente a biopsias mamarias, consistente en una mesa prona (la paciente está acostada en decúbito ventral), la mama pasa por un orificio amplio en la mesa y la biopsia se realiza debajo de la mesa, donde se encuentra el equipo mamográfico, no visualizable para la paciente acostada, por lo que las posibilidades de movimiento y reacción vagal son mucho menores.
Para la toma del material histológico se utilizó una pistola automática con sistema de resortes y agujas de 18G, el mismo calibre usado para la toma de biopsias de próstata, en las primeras 65 biopsias, pero dado que la mama contiene mayor cantidad de tejido adiposo, el material no resultó satisfactorio para los patólogos. Las siguientes 9 biopsias se realizaron con agujas de 16G que tampoco fue adecuado y las últimas 29 se realizaron con agujas de 14G quedando satisfechos los patólogos con el material obtenido.
Al año siguiente, el mismo Dr. Steve Paker, publica su serie de biopsias en 102 pacientes, siguiendo una técnica estandarizada: biopsia estereotáxica en mesa prona, aguja de 14G y pistola automática de larga excursión (23 mm), con excelentes resultados3. Unos años más tarde surgieron las biopsias con sistema de vacío, inicialmente con agujas de 14G y luego de 11G, que demostraron beneficios y se consagraron como el método ideal para lesiones principalmente vinculadas a microcalcificaciones, por presentar menor subestimaciones y falsos negativos4.
El análisis de numerosas series demostró que las biopsias por punción son certeras (sensiblilidad ≥ 97%) 5 y seguras (complicaciones ≤1.5%), con mejor cosmesis y menores costos que las biopsias quirúrgicas.
También, se demostró que cuando se realizaba biopsia por punción inicialmente se conseguía terapéutica en un solo tiempo quirúrgico en mayor porcentaje que cuando se realizaba biopsia quirúrgica inicialmente6 y la indicación del estudio del ganglio centinela como el método habitual para la investigación axilar en pacientes con cáncer de mama y axilas clínicamente negativas7, consolidaron a las biopsias por punciónhistológicas guiadas por imágenes como la primeraindicación de biopsia en lesiones mamarias sospechosas8.
La tecnología digital, con un campo parcial de 5×5 cm, llegó en 1993, antes para las mesas de biopsia pronas que para los equipos mamográficos.
La mamografía digital de campo completo fue aprobada en el año 2000, pero no tuvo impacto significativo hasta el año 2005 cuando se publicó el estudio DMIST9, luego del cual se produjo una rápida migración hacia la mamografía digital de campo completo (digital directa o indirecta, según cada país). La plataforma digital fue fundamental para el desarrollo de la tomosíntesis, que fue aprobada en 2011.
La tomosíntesis demostró incremento en la detección de carcinomas, aproximadamente 40% y disminución en la recitación o rellamados de aproximadmente 15%, comparativamente con la mamografía digital.10-12
Si bien muchas de las lesiones sospechosas detectadas por tomosíntesis, no visibles en la mamografía, son visibles ecográficamente y es posible realizar su biopsia mediante este método, hay lesiones que son solamente visibles en tomosíntesis. Dada la falta de equipamiento adecuado para realizar biopsias por tomosíntesis cuando el método surgió al mercado, diferentes soluciones fueron adoptadas13-17.
La introducción de la mamografía digital directa determinó un significativo incremento en la detección de microcalcificaciones18, muchas de ellas difíciles de identificar en los equipos de estereotaxia con tecnología más antigua.
La primera solución para estos problemas llegó el año 2013, cuando Hologic presentó el Affirm®, un sistema de biopsia con tomosíntesis que se adosa al equipo mamográfico (sistema add-on).
El método fue muy bien recibido, demostrando ser certero, seguro. Además, gracias al detector de alta resolución, a su campo de visualización de la imagen mayor a 5×5 cm y a su capacidad de tomosíntesis, la detección de las lesiones fue más rápida que con los equipos antiguos19, 20.
Tres años después, se presentó la mesa prona con capacidad de tomosíntesis. En palabras de las más altas autoridades de Hologic: “El lanzamiento de la mesa prona Affirm Prone® es el avance más significativo en tecnología de mesa prona desde que lanzamos la primera mesa hace más de 20 años atrás” 21.

En el mes de Mayo de 2017 recibimos las dos primeras mesas pronas con tomosíntesis instaladas en América fuera de EE.UU. y Canadá.

Quisiera compartir con ustedes nuestra experiencia con estos equipos en los primeros diez meses de utilización (2/5/17 al 28/2/18), en los que realizamos 2808 biopsias.
Los conceptos que se relatan surgen de las opiniones de los seis médicos que realizan las biopsias diariamente en CERIM (Buenos Aires), consultados mediante una encuesta anónima.
El equipo presenta mejoras en el confort de la paciente, con acolchado más grueso y confortable, orificio para posicionamiento de las mamas de mayor tamaño, lo que facilita el descenso del brazo cuando es necesario, contando además con un apoyabrazos para estas ocasiones. Algunas pacientes siguen quejándose de molestias en el cuello porque la posición es igual.
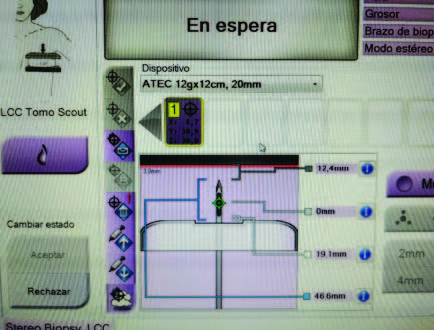
La consola presenta cambios sustanciales, con importantes mejoras: no es necesario calcular el “0” antes de empezar cada procedimiento, simplemente, luego de determinar la ubicación de la lesión en un solo punto en el espacio, con tomosíntesis, nos muestra las coordenadas X, Y y Z de la lesión y basta con seleccionar que aguja utilizaremos para esta biopsia, de una lista con todos los tipos de agujas que utilizamos habitualmente, para que el equipo automáticamente nos indique en un gráfico: la posición que tendrá la aguja dentro de la mama, su relación con la lesión, el compresor y el detector, alertándonos con colores amarillo y rojo cuando la distancia al mismo es escasa o insuficiente (imagen).
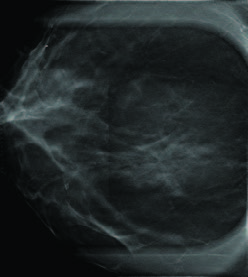
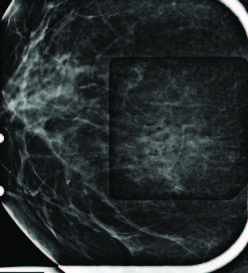
La facilidad para detectar las lesiones, debido al amplio campo de visualización con compresores acrílicos transparentes y la alta resolución de las imágenes gracias al detector de gran resolución, son sin duda las cualidades más destacadas y valoradas del equipo, que generan dos nuevas virtudes: reducción del tiempo necesario para realizar las biopsias y mayor certeza al identificar las lesiones.
Las complicaciones de las biopsias, muy poco frecuentes a excepción de las vinculadas al sangrado, no se han modificado respecto del equipamiento previo.
La capacidad de biopsiar lesiones mediante tomosíntesis, más allá de la imperiosa necesidad del método para las lesiones solamente detectadas por tomosíntesis, presenta dos grandes ventajas, inexistentes anteriormente:
1- simplificación y mayor precisión al localizar la lesión en un único punto en el espacio (mayor precisión que mediante estereotaxia: necesita seleccionar dos puntos idénticos de la lesión el espacio).
2- Menor dosis de radiación:
En cada incidencia mamográfica scout (directa) la dosis de radiación es 1.6 mGy, en estereotaxia (son necesarias dos incidencias) la dosis total es 3.2 mGy y la dosis de una adquisición con tomosíntesis es 1.8 mGy. Por lo tanto, cada vez que se utilice tomosíntesis en reemplazo de estereotaxia (calcular la ubicación de la lesión, pre-disparo, post-disparo o al finalizar la toma de las muestras, se estará utilizando una dosis de radiación 1.4 mGy menor (44% de reducción) si se realiza con tomosínteis en lugar de estereotaxia.
De todas formas, el sistema posee las dos opciones (tomosíntesis y estereotaxia) siendo algunas variantes muy frecuentemente utilizadas por algunos operadores. Ej: calcular la localización de la lesión con tomosíntesis y comprobar la relación entre la aguja y la lesión (pre-disparo) mediante estereotaxia.
Adicionalmente, la tomosíntesis nos permite identificar, rápida y certeramente, calcificaciones de dependencia dérmica y en algunos casos, estructuras vasculares que están cerca de la lesión o en el trayecto de la aguja entre la piel y la lesión para poder modificar nuestra aproximación a la lesión y evitar sangrados.
Finalmente, el equipo presenta la posibilidad de acceso lateral, muy útil en mamas con muy escaso espesor al realizar la compresión, donde no es posible la biopsia de otra forma. El sistema funciona muy bien y no son necesarios cálculos sofisticados, el equipo hace su re-cálculo automáticamente y nos indica por donde debemos ingresar, así como las conocidas coordenadas de la lesión.
En resumen, la nueva mesa prona con capacidad de biopsia por tomosíntesis llega como una necesidad para poder realizar biopsias en lesiones solamente visibles por este método, pero claramente representan un importantísimo salto de calidad en la identificación de las lesiones, con significativas mejoras en la certeza para la realización de las mismas, en las reducciones del tiempo necesario para cada procedimiento y la dosis de radiación y mayor confort para la paciente. Además de la alternativa de un acceso lateral cuando el escaso espesor mamario luego de la compresión no permiten un acceso convencional. Las mayores comodidades para la paciente y el operador respecto de los equipos que se agregan a los mamógrafos (add-on), con menores posibilidades de que la paciente se mueva o presente una reacción vagal convierten a la nueva mesa prona en el estándar de oro (gold standard) para la realización de biopsias guiadas por estereotaxia y/o tomosínteisis.
*Este artículo expresa la opinión de un usuario del producto Affirm Prone® experto en el procedimiento de biopsia. Para informaciones adicionales y detalles técnicos acerca del producto, por favor contactar el representante Hologic autorizado en su país.
Bibliografía
1. Hayes MK. Update on Preoperative Breast Localization. Radiol Clin North Am. 2017; 55 (3) : 591-603.
2. Parker SH, Lovin JD, Jobe WE, et al. Stereotactic Breast Biospsy with a Biopsy Gun. Radiology 1990; 176:741-747.
3. Parker SH, Lovin JD, Jobe WE, et al. Nonpalpable Breast Lesions: Stereotactic Automated Large-Core Biopsies. Radiology 1991; 180:403-407.
4. Bassett LW, Mahoney MC, Apple SK. Interventional breast imaging: current procedures and assessing for concordance with pathology. Radiol Clin North Am. 2007; 45 (5):881-94.
5. Dahabreh IJ, Wieland LS, Adam GP, Halladay C, Lau J, Trikalinos TA. Core Needle and Open Surgical Biopsy for Diagnosis of Breast Lesions: An Update to the 2009 Report. Comparative Effectiveness Review No. 139. (Prepared by the Brown Evidence-based Practice Center under Contract 290-2012-00012-I.) AHRQ Publication No. 14-EHC040-EF. Rockville, MD: Agency for Healthcare Research and Quality. September 2014.
6. Liberman L, Goodstine SL, Dershaw DD, Morris EA, LaTrenta LR, Abramson AF, Van Zee KJ. One operation after percutaneous diagnosis of nonpalpable breast cancer: frequency and associated factors. AJR Am J Roentgenol. 2002 Mar;178 (3):673-9.
7. Peters-Engl C, Konstantiniuk P, Tausch C, Haid A, Hoffmann B, Jagoutz-Herzlinger M, Kugler F, Redtenbacher S, Roka S, Schrenk P, Steinmassl D; Austrian Sentinel Node Biopsy Study Group. The impact of preoperative breast biopsy on the risk of sentinel lymph node metastases: analysis of 2502 cases from the Austrian Sentinel Node Biopsy Study Group. Br J Cancer. 2004; 91 (10):1782-6.
8. van Breest Smallenburg V, Nederend J, Voogd AC, Coebergh JW, van Beek M, Jansen FH, Louwman WJ, Duijm LE. Trends in breast biopsies for abnormalities detected at screening mammography: a population-based study in the Netherlands. Br J Cancer. 2013;109 (1):242-8.
9. Pisano ED, Gatsonis C, Hendrick E, Yaffe M, Baum JK, Acharyya S, Conant EF, Fajardo LL, Bassett L, D’Orsi C, Jong R, Rebner M; Digital Mammographic Imaging Screening Trial (DMIST) Investigators Group. Diagnostic performance of digital versus film mammography for breast-cancer screening. N Engl J Med. 2005 Oct 27;353 (17):1773-83.
10. Skaane P, Bandos AI, Gullien R, Eben EB, Ekseth U, Haakenaasen U, Izadi M, Jebsen IN, Jahr G, Krager M, Niklason LT, Hofvind S, Gur D. Comparison of digital mammography alone and digital mammography plus tomosynthesis in a population-based screening program. Radiology. 2013 Apr;267 (1):47-56.
11. Ciatto S, Houssami N, Bernardi D, Caumo F, Pellegrini M, Brunelli S, Tuttobene P, Bricolo P, Fantò C, Valentini M, Montemezzi S, Macaskill P. Integration of 3D digital mammography with tomosynthesis for population breast-cancer screening (STORM): a prospective comparison study. Lancet Oncol. 2013 Jun;14 (7):583-9.
12. Friedewald SM, Rafferty EA, Rose SL, Durand MA, Plecha DM, Greenberg JS, Hayes MK, Copit DS, Carlson KL, Cink TM, Barke LD, Greer LN, Miller DP, Conant EF. Breast cancer screening using tomosynthesis in combination with digital mammography. JAMA. 2014 Jun 25;311 (24):2499-507.
13. Taskin F, Durum Y, Soyder A, Unsal A. Review and management of breast lesions detected with breast tomosynthesis but not visible on mammography and ultrasonography. Acta Radiol. 2017 Dec;58 (12):1442-1447.
14. Freer PE, Niell B, Rafferty EA. Preoperative Tomosynthesis-guided Needle Localization of Mammographically and Sonographically Occult Breast Lesions. Radiology. 2015 May;275(2):377-83.
15. Roth RG, Maidment AD, Weinstein SP, Roth SO, Conant EF. Digital breast tomosynthesis: lessons learned from early clinical implementation. Radiographics. 2014 Jul-Aug;34 (4):E89-102.
16. Slanetz PJ, Brown AL, Bradley M, Karimova EJ. Tomosynthesis-Directed Coaxial Core Biopsy of Tomosynthesis-Detected Architectural Distortion: Indications and Logistics. Can Assoc Radiol J. 2017 Aug;68 (3):315-317.
17. Viala J, Gignier P, Perret B, Hovasse C, Hovasse D, Chancelier-Galan MD, Bornet G, Hamrouni A, Lasry JL, Convard JP. Stereotactic vacuum-assisted biopsies on a digital breast 3D-tomosynthesis system. Breast J. 2013 Jan-Feb;19 (1):4-9.
18. Del Turco MR, Mantellini P, Ciatto S, Bonardi R, Martinelli F, Lazzari B, Houssami N. Full-field digital versus screen-film mammography: comparative accuracy in concurrent screening cohorts. AJR Am J Roentgenol. 2007 Oct;189(4):860-6.
19. Schrading S, Distelmaier M, Dirrichs T, Detering S, Brolund L, Strobel K, Kuhl CK. Digital breast tomosynthesis-guided vacuum-assisted breast biopsy: initial experiences and comparison with prone stereotactic vacuum-assisted biopsy. Radiology. 2015 Mar;274(3):654-62.
20. Waldherr C, Berclaz G, Altermatt HJ, Cerny P, Keller P, Dietz U, Buser K, Ciriolo M, Sonnenschein MJ. Tomosynthesis-guided vacuum-assisted breast biopsy: A feasibility study. Eur Radiol. 2016 Jun;26(6):1582-9.
21. www.mpo-mag.com/contents/view_breaking-news/2016-04-22/fda-clears-hologic-prone-biopsy-system