De un vistazo
El análisis de deep learning de las radiografías de tórax iniciales puede facilitar una clasificación más eficiente de los pacientes que llegan a lsa sala de emergencias con dolor torácico agudo.
El modelo de deep learning mejoró significativamente la predicción del síndrome coronario agudo, la embolia pulmonar y la disección aórtica.
El síndrome de dolor torácico agudo representa más de 7 millones de visitas al departamento de emergencias anualmente en los Estados Unidos, lo que lo convierte en una de las quejas más comunes.
La inteligencia artificial (IA) puede ayudar a mejorar la atención de los pacientes que acuden al hospital con dolor torácico agudo, según un estudio publicado en Radiology, una revista RSNA.
“Hasta donde sabemos, nuestro modelo de IA de deep learning es el primero en utilizar radiografías de tórax para identificar a los pacientes con dolor torácico agudo que necesitan atención médica inmediata”, dijo el autor principal del estudio, Márton Kolossváry, MD, Ph. D., investigador de radiología en el Hospital General de Massachusetts (MGH) en Boston.

El síndrome de dolor torácico agudo puede consistir en opresión, ardor u otra molestia en el pecho o un dolor intenso que se extiende a la espalda, el cuello, los hombros, los brazos o la mandíbula. Puede ir acompañada de dificultad para respirar.

El síndrome de dolor torácico agudo representa más de 7 millones de visitas al departamento de emergencias anualmente en los Estados Unidos, lo que lo convierte en una de las quejas más comunes. Menos del 8% de estos pacientes son diagnosticados con las tres principales causas cardiovasculares del síndrome de dolor torácico agudo, que son el síndrome coronario agudo, la embolia pulmonar o la disección aórtica. Sin embargo, la naturaleza potencialmente mortal de estas afecciones y la baja especificidad de las pruebas clínicas, como los electrocardiogramas y los análisis de sangre, conducen a un uso considerable de diagnóstico por imágenes cardiovascular y pulmonar, que a menudo arroja resultados negativos. Dado que los departamentos de emergencia luchan con un gran número de pacientes y la escasez de camas de hospital, es importante clasificar de manera efectiva a los pacientes con un riesgo muy bajo de estas afecciones graves.
El deep learning es un tipo avanzado de inteligencia artificial (IA) que se puede entrenar para buscar imágenes de rayos X para encontrar patrones asociados con enfermedades.
Para el estudio, el Dr. Kolossváry y sus colegas desarrollaron un modelo de deep learning de código abierto para identificar a los pacientes con síndrome de dolor torácico agudo que estaban en riesgo de síndrome coronario agudo de 30 días, embolia pulmonar, disección aórtica o mortalidad por todas las causas, según una radiografía de tórax.
El estudio utilizó historias clínicas electrónicas de pacientes que presentaban síndrome de dolor torácico agudo a los que se les realizó una radiografía de tórax e imágenes cardiovasculares o pulmonares adicionales y/o pruebas de esfuerzo en MGH o en el Brigham and Women’s Hospital de Boston entre enero de 2005 y diciembre de 2015. En este estudio se evaluaron 5.750 pacientes (edad media 59, incluidos 3.329 hombres).
El modelo de deep learning se entrenó en 23 005 pacientes de MGH para predecir un criterio de valoración compuesto de 30 días de síndrome coronario agudo, embolia pulmonar o disección aórtica y mortalidad por todas las causas según las imágenes de rayos X de tórax.
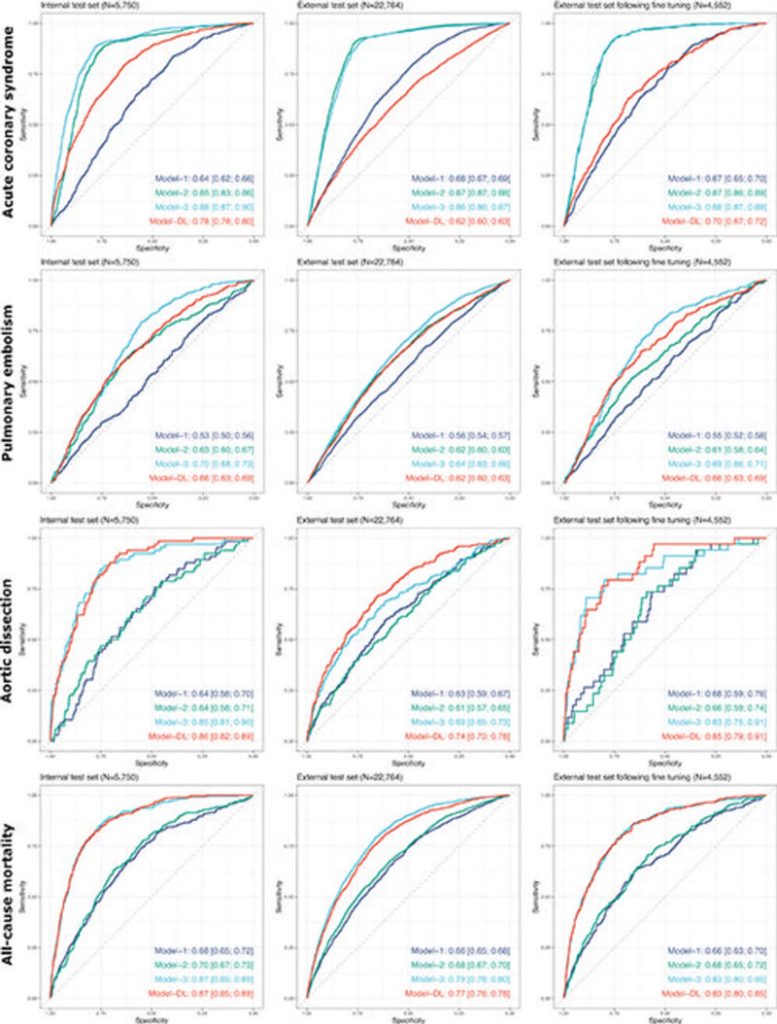
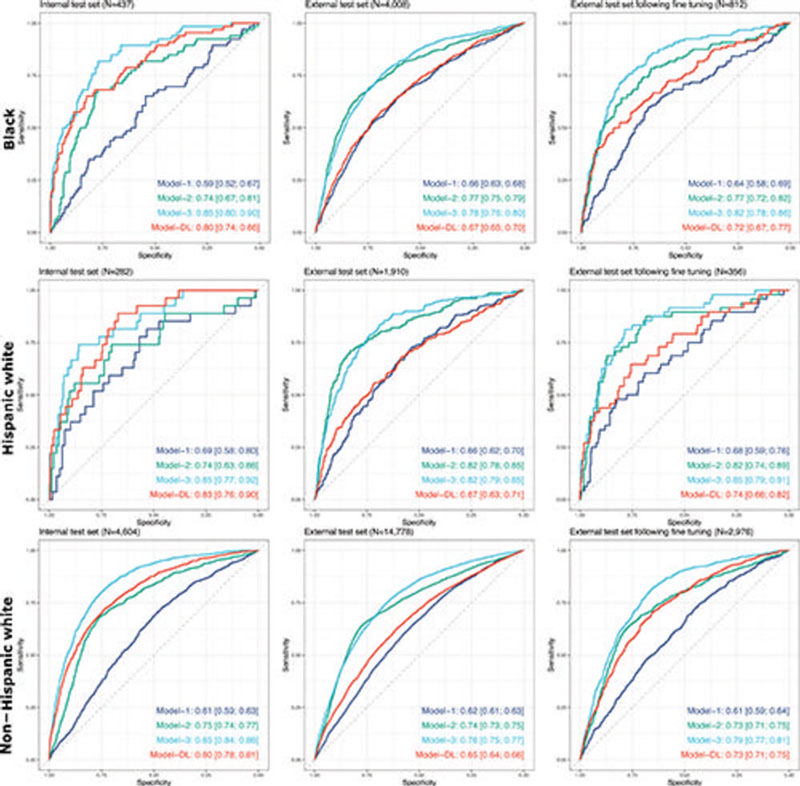
La herramienta de deep learning mejoró significativamente la predicción de estos resultados adversos más allá de la edad, el sexo y los marcadores clínicos convencionales, como los análisis de sangre del dímero D. El modelo mantuvo su precisión diagnóstica en función de la edad, el sexo, el origen étnico y la raza. Con un umbral de sensibilidad del 99 %, el modelo pudo diferir las pruebas adicionales en el 14 % de los pacientes en comparación con el 2 % cuando se usaba un modelo que solo incorporaba datos de edad, sexo y biomarcadores.
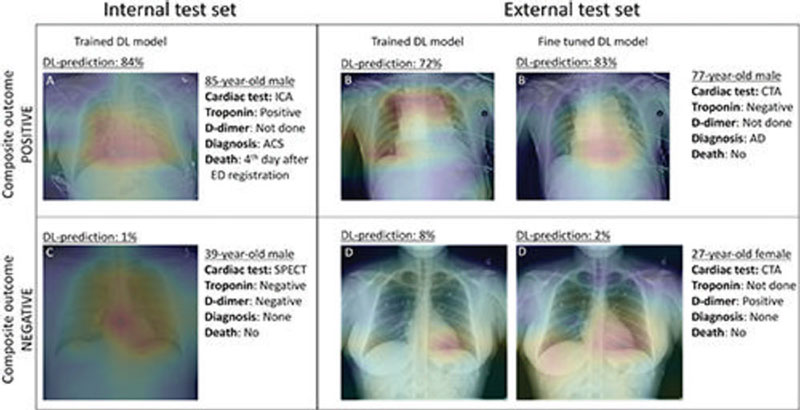
“Al analizar la radiografía de tórax inicial de estos pacientes con nuestro modelo de deep learning automatizado, pudimos proporcionar predicciones más precisas sobre los resultados de los pacientes en comparación con un modelo que utiliza información sobre la edad, el sexo, la troponina o el dímero D”, dijo el Dr. Kolossváry “Nuestros resultados muestran que las radiografías de tórax podrían usarse para ayudar a clasificar a los pacientes con dolor de pecho en el departamento de emergencias”.
Según el Dr. Kolossváry, en el futuro, un modelo automatizado de este tipo podría analizar las radiografías de tórax en segundo plano y ayudar a seleccionar a aquellos que se beneficiarían más de la atención médica inmediata y podría ayudar a identificar a los pacientes que pueden ser dados de alta del departamento de emergencias de manera segura.

