Reporte de un caso
Autores: Romina Lorena Romero1, César Mendez1, Karina Quintero Rodriguez2, María del Carmen Alak1.
- Servicio de Medicina Nuclear Hospital Británico de Buenos Aires, Buenos Aires, Argentina.
- Servicio de Medicina Nuclear Hospital Nacional de Pediatría Garrahan, Buenos Aires, Argentina.
Contacto: romeroromina1125@gmail.com
Conflicto de interés: los autores declaran no tener ningún conflicto de interés.
Introducción
La visualización de órganos diferentes al pulmón en los estudios de ventilación/perfusión (V/Q) pulmonar, en la fase perfusoria por captación del 99mTC-macroagregados es algo inusual, pero se conoce, y hay casos reportados con anterioridad en la literatura.
Descripción del caso
Paciente femenina de 30 años. Con antecedente de LH diagnosticado hace 10 años. Recibió quimioterapia y radioterapia en cuello como tratamiento. Se realizó trasplante autólogo de médula ósea por recaída 8 años después.
Actualmente en remisión.
Concurre a la consulta por disnea progresiva a mínimos esfuerzos, de 1 mes de evolución aproximadamente. Al examen físico se evidencia eritema y edema de miembros superiores a predominio derecho y en cara. Ingurgitación yugular con el decúbito dorsal. Tolera el decúbito. Saturación 99% con FIO2 0.21%. Laboratorio normal.
Se realiza eco Doppler cardíaco: FSVI conservada. Fey 58% FSVD conservada.
PSAP 22 mmHg. Sin signos indirectos de HTP significativa.
PET previo (no se dispone de las imágenes): Imagen con defecto de relleno en relación con el extremo distal del catéter intravascular localizado en el origen de la vena cava superior,
que impresiona corresponder a trombo sin condicionar el flujo vascular.
Eco Doppler de Miembro superior derecho: Negativo para TVP en relación al Portacath.
Se solicita centellograma V/Q para descartar presencia de TEP: se procedió a realizar la ventilación con 20 mCi de TC99m DTPA y adquisición de imágenes, y posteriormente se
procedió a la etapa de perfusión, con inyección endovenosa de 5mCI Tc99m macroagregados (MAA-Tc99m) y adquisición de imágenes planares y en modo SPECT de pulmón.
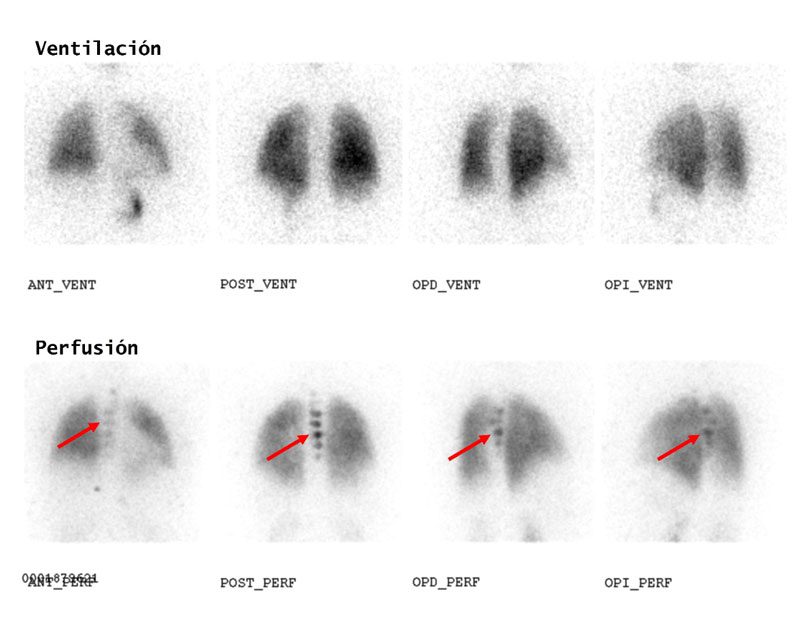
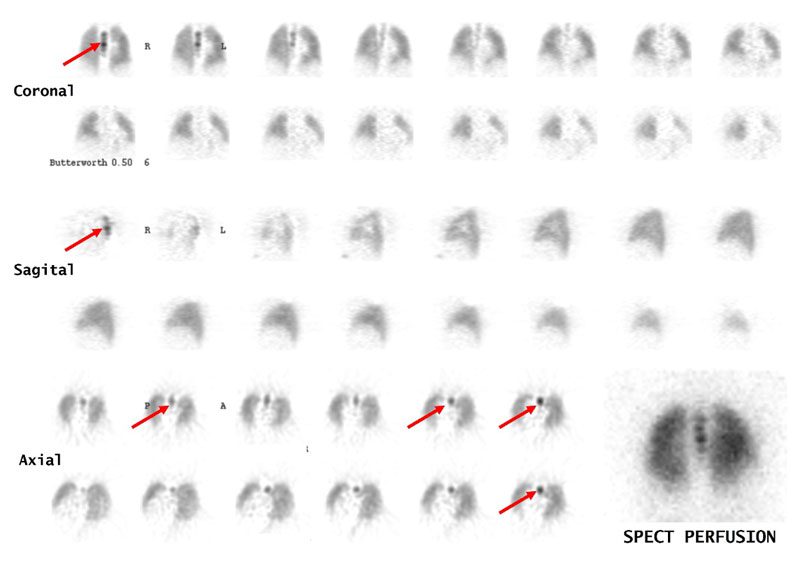
En las imágenes de ventilación no se observan áreas netas diferenciables en la distribución del radio-aerosol, al igual que en la secuencia de imágenes perfusorias planares y SPECT, que no evidenciaron defectos segmentarios sugestivos de TEP.
Llama la atención, en las adquisiciones de perfusión, la presencia de captación anómala del MAA-Tc99m proyectada posteriormente en la línea media superior de la caja torácica, en relación de vértebras torácicas.
Esta captación es esperable visualizarla en las imágenes ventilatorias de este estudio por deglución del trazador en esófago o depósito en vía aérea principal, pero no en la etapa
perfusoria (Fig. 1 y 2).
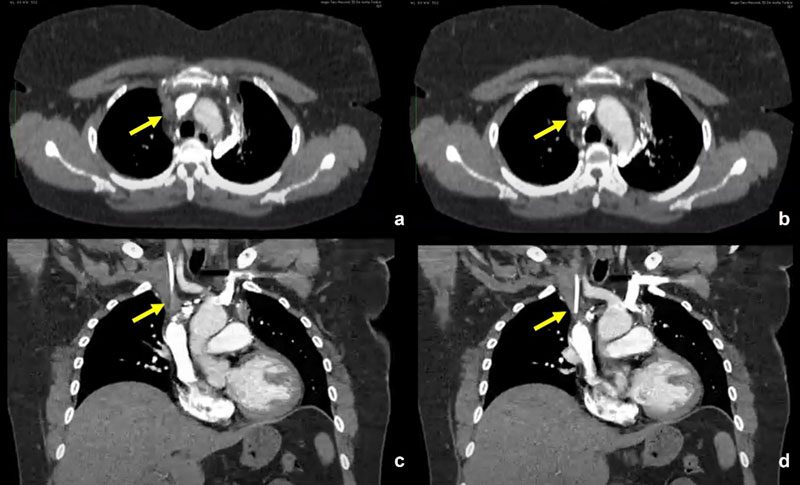
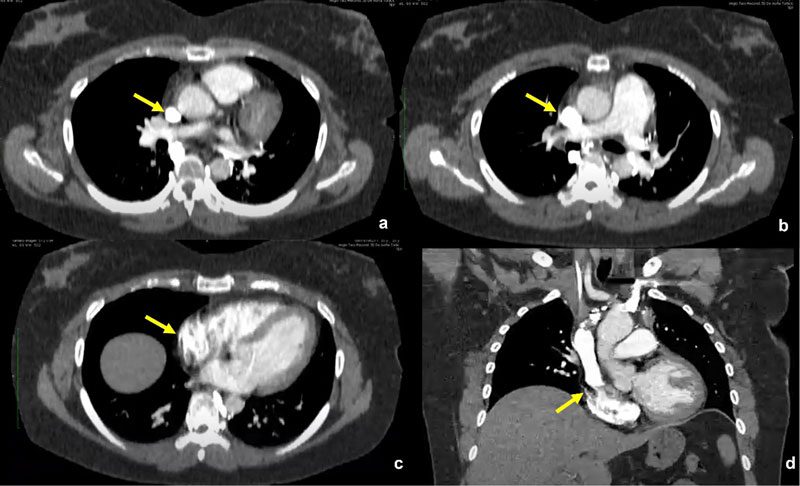
Se decidió realizar Angiotac: No impresiona TEP. Se destaca defecto de relleno en porción proximal de vena cava superior sugestiva de trombosis, posterior al extremo distal del catéter de infusión (Fig. 3).
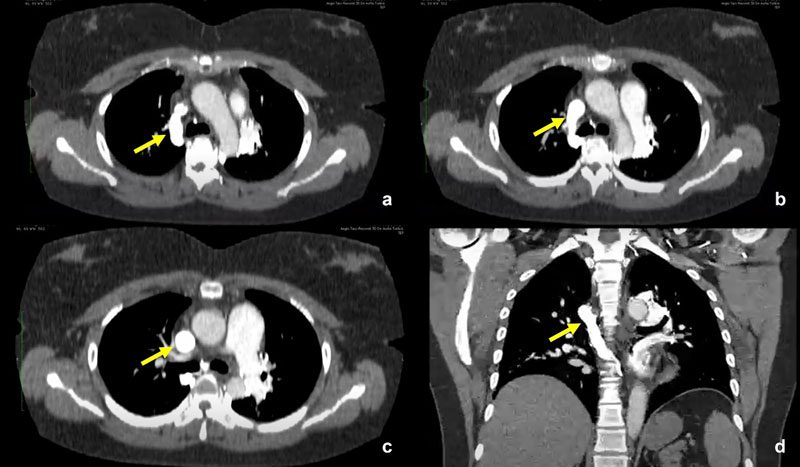
Se detectó también circulación colateral hiliar bilateral con drenaje en sistema ácigos mayor y menor (Fig. 4, 5 y 6).
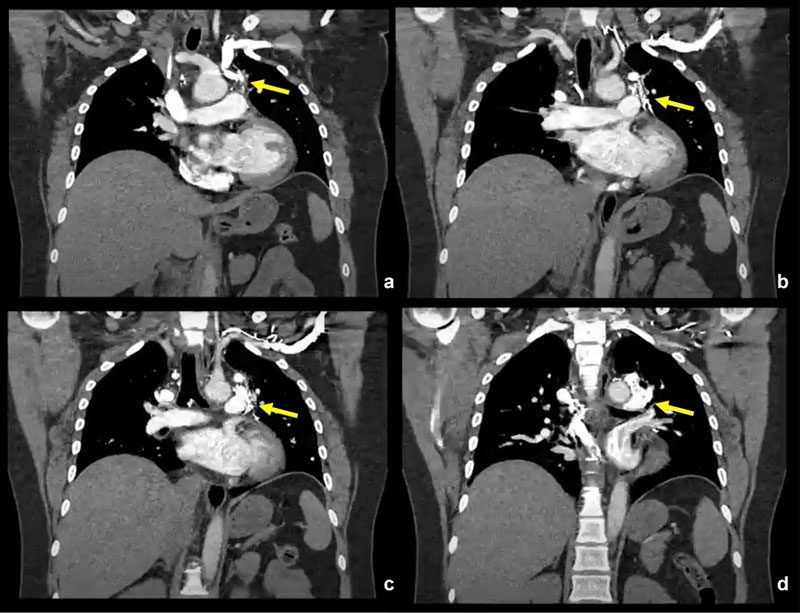
Se inició tratamiento con rivaroxabán (antitrombótico) y manejo clínico de la paciente.
Discusión
Aunque poco común, es conocido que en estudios de perfusión pulmonar con Tc99m-MAA puede observarse la visualización de órganos distintos al pulmón debido al paso del radiofármaco a la circulación sistémica. Esta situación ha sido previamente documentada en la literatura médica (1,4).
En presencia de una obstrucción en la Vena Cava Superior (VCS), se vuelve muy importante la formación de vías alternativas para mantener el drenaje venoso. Estas vías
ayudan a prevenir un empeoramiento del cuadro clínico del paciente y pueden explicar la aparición de captaciones extrapulmonares del MAA en lugares inusuales como el hígado,
el esternón, las vértebras, los arcos costales, el cerebro y los riñones, en un estudio de perfusión pulmonar, como se ha descrito en casos previos (1,2,3).
El desarrollo de esas vías colaterales o alternas ayuda a llevar la sangre venosa de la parte superior del cuerpo hacia el corazón derecho, pudiendo depositarse el MAA en la primera red capilar que encuentra. Algunas de estas vías colaterales son las intercostales superiores e inferiores, la mamaria interna, el sistema venoso vertebral, la vena ácigos y la hemiácigos (2).
En nuestro caso, la visualización de las vértebras torácicas se debe al flujo retrógrado a través del sistema venoso vertebral dilatado, que normalmente lleva la sangre venosa
prevertebral al sistema ácigos, y también al nulo drenaje de la médula ósea, donde el MAA queda atrapado (2,4).
La obstrucción de la VCS es una complicación conocida debido a la trombosis que se genera alrededor del catéter venoso central (causa benigna), pero la mayoría de las obstrucciones de la VCS es debido a causas malignas (85-90% de los casos), por lo que hay que estudiar el motivo que la produjo, siendo importante completar la valoración con un método anatómico como lo es la TC con contraste endovenoso (4,5).
Es importante tener en cuenta que el desarrollo de estas vías colaterales puede variar según el nivel de obstrucción y pueden tener diferentes patrones (Tabla 1). La formación
de una vía venosa colateral sistémica a pulmonar es una complicación poco común de la obstrucción de la VCS. La presencia de tales vasos colaterales da como resultado un
cortocircuito de derecha a izquierda, lo que puede dejar al paciente susceptible a un accidente cerebrovascular, absceso cerebral y un estado de alto gasto cardíaco (4).
En nuestro caso, se evidenció un shunt de derecha a izquierda, como se describe en la Fig. 6. Ya que el diagnóstico era reciente, la paciente aún no presentaba signos instalados de hipertensión pulmonar. De igual forma, se tomaron medidas para controlar el flujo sanguíneo, la presión arterial y evitar posibles complicaciones.
Otros de los sitios donde se puede llegar acumular MAA durante un estudio de perfusión en el contexto de una trombosis de VCS es el hígado: en caso de que el sistema ácigos se involucre, las vías colaterales de la pared torácica y la parte superior del abdomen desviarán el flujo de sangre al corazón, pudiéndose generar una comunicación entre estas vías colaterales y la vena umbilical o paraumbilical (que se re-permeabiliza) pudiéndose llegar a formar una derivación a la vena porta. En su mayoría, este drenaje se realiza en la rama principal izquierda de la vena porta y el MAA queda atrapado en una parte del lóbulo hepático izquierdo (4,6).
Referencias
- Karls S, Hassoun H, Derbekyan V. Vertebral Uptake of Tc-99m Macroaggregated Albumin (MAA) with SPECT/CT Occurring in Superior Vena Cava Obstruction. Nucl Med Mol Imaging.
2016;50(3):266-269. doi:10.1007/s13139-015-0372-y. - Esser JP, Oei HY, de Bruin HG, Krenning EP. Liver and vertebral uptake of Tc-99m macroaggregated albumin (MAA). Clin Nucl Med. 2004;29(12):793-794. doi:10.1097/00003072-200412000-00004.
- Meristoudis G, Ilia I, Tsaroucha A, Giannakopoulos V, Christakopoulou J. Liver and vertebral visualization on lung perfusion scan. Rev Esp Med Nucl. 2008;27(5):369. doi:10.1157/13126195.
- Kapur S, Paik E, Rezaei A, Vu DN. Where there is blood, there is a way: unusual collateral vessels in superior and inferior vena cava obstruction. Radiographics. 2010;30(1):67-78. doi:10.1148/ rg.301095724.
- Grayet D, Ghaye B, Szapiro D, Dondelinger RF. Systemic-to-pulmonary venous shunt in superior vena cava obstruction revealed on dynamic helical CT. AJR Am J Roentgenol. 2001;176(1):211-213. doi:10.2214/ajr.176.1.1760211.
- Ramos Font C, Sánchez de Mora E, López Martín J, Salgado-García C, Lerma del Vallle MD, Jiménez Hefferman A. Captación extrapulmonar de macroagregados de albúmina marcada con Tc99m en un estudio de ventilación-perfusión. Rev Esp Med Nucl Imagen Mol. 2013;32(2):130-131. doi:10.1016/j.remn.2012.05.001. Tabla 1. Vías venosas colaterales ante obstrucciones de VCS y de VCI.

